
第一作者:武龙胜
通讯作者:胡敬平
论文引用:Electrochimica Acta, 2023,466,142973
论文DOI:10.1016/j.electacta.2023.142973
论文全文链接:https://doi.org/10.1016/j.electacta.2023.142973
FunMat课题组主页:http://funmat.ese.hust.edu.cn/
近日,华中科技大学环境学院Funmat课题组胡敬平教授团队与英国牛津大学John Foord教授和比利时Hasselt大学Ken Haenen教授团队合作,在Electrochimica Acta 上发表了题为“Lithium nitrate mediated dynamic formation of solid electrolyte interphase revealed by in situ Fourier transform infrared spectroscopy”的研究论文(Electrochimica Acta, 2023,466,142973, DOI:10.1016/j.electacta.2023.142973)。论文首次通过原位傅立叶变换红外光谱(FTIR)和从头算分子动力学(AIMD)方法揭示了硝酸锂(LiNO3)添加剂对锂阳极表面SEI动态演化的影响机制。FTIR和AIMD结果直接表明,LiNO3可以加速双(三氟甲基磺酰基)酰亚胺锂(LiTFSI)在锂阳极上还原为富含Li2O的小分子物质,从而在浸没在含LiNO3的电解质后形成致密稳定的SEI。由于SEI的稳定性,LiTFSI和溶剂在随后的锂沉积溶出过程中分解受到阻碍,从而促使产生更高的库仑效率和长期循环稳定性。此外,在锂沉积过程中也观察到一种类ROSO2Li中间体,同时在锂溶出过程中分解或扩散,从而维持了SEI的动态形成/溶解平衡。这项研究为阐释LiNO3在稳定锂电极中的作用提供了新的视角。
引言
稳定的固体电解质界面(SEI)在高性能锂硫(Li-S)电池的循环稳定性和库仑效率(CE)中起着至关重要的作用。LiNO3添加剂的作用已被广泛探索,其中大多数研究是通过非原位技术进行的,很难感知可溶性物质和界面动态变化。此外,由于锂电极的高反应性,在样品后处理过程中可能会发生一些不良反应,从而破坏结果的可靠性。此外,理论计算还可以为SEI的形成机理提供新见解。本文通过在1M LiTFSI-DOL/DME (1:1,v/v)电解质中的原位FTIR实验和理论计算,探讨了SEI在电解质/电极界面上的生成机理和动力学行为,以及LiNO3添加剂对SEI性能的影响。用纽扣电池测定了不同电解质体系中循环锂的电化学性能,并对循环锂电极的形貌进行了表征。此外,利用原位红外光谱研究了LiNO3在电解质/电极界面上的动态行为及其SEI特性的影响。此外,通过AIMD模拟比较了有无LiNO3添加剂时锂离子在锂表面的还原过程。这项研究为进一步研究LiNO3在SEI形成机理和锂电极电化学性能中的作用提供了新的视角。
图文导读
一、电化学性能
在1 M LiTFSI-DOL/DME电解质中加入2 wt% LiNO3可显著改善锂沉积/剥离的CE和长期循环稳定性。在没有添加剂的情况下,锂沉积/溶出的初始CE为69%,并且在第5 ~ 30个循环中CE保持稳定(> 90%)。然而,CE在随后的170个周期中变得波动(图1a)。在电解液中加入2 wt% LiNO3,锂沉积/溶出的CE达到94%,并在随后的200个循环中保持高值(> 90%)(图1a)。另外,用Li| |Li电池测量了锂阳极在不同电解质中的循环稳定性(图1b)。在1 M LiTFSI-DOL/DME电解质中,无LiNO3电池的极化电位在130 h后升高,500 h后达到0.2 V。相比之下,在电解液中加入2%的LiNO3,极化电位在整个1000 h内保持稳定,表明循环寿命更长。电化学性能表明,在电解质中加入LiNO3提高了锂电极的CE和循环稳定性。电池的CE和极化主要受锂和电解质组分反应产生的锂的SEI的影响。
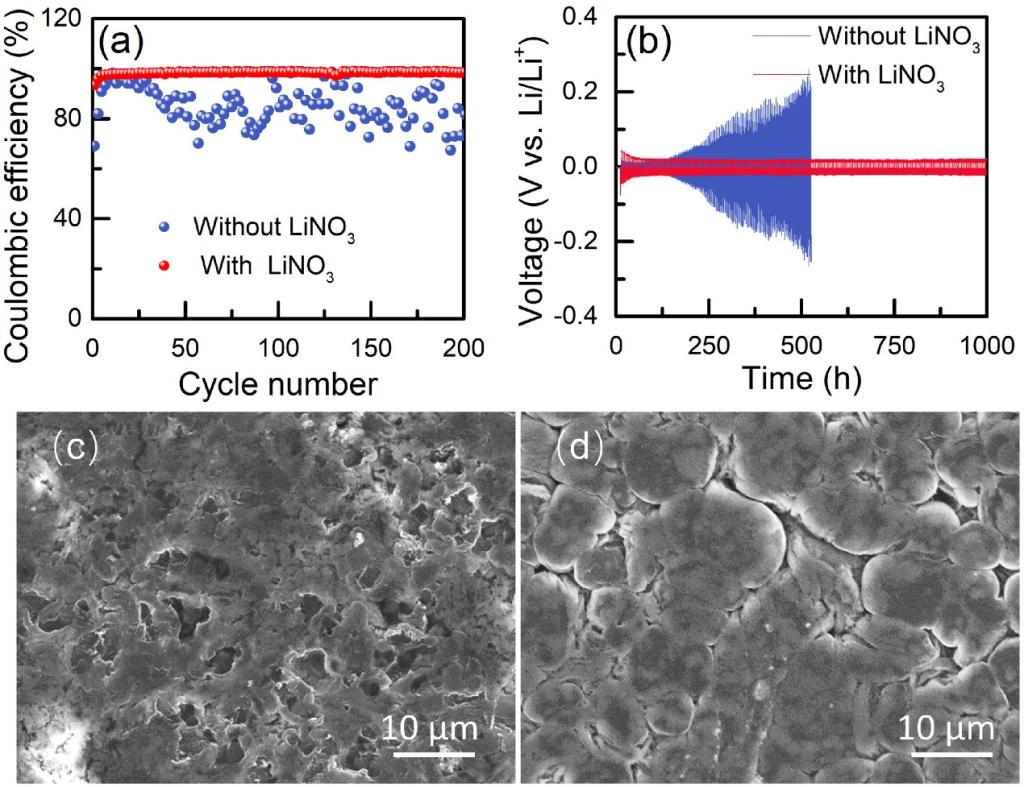
图 1. (a) 不同电解质中Li| |Cu电池的库仑效率测量。将Li以0.5 mA cm-2沉积在Cu上以1 mAh cm-2沉积容量,然后以0.5 mA cm-2剥离至0.5 V的截止电压。(b) 在0.5 mA cm-2循环至1 mAh cm-2的不同电解质中的Li| |Li电池的电位曲线。在电解质中循环100次后,Li| |Li电池循环Li表面的SEM图像:(c) DOL/DME中的1 M LiTFSI,(d) DOL/DME中的1 M LiTFSI和2 wt% LiNO3。
二、循环锂的形貌表征
对100次循环后锂电极的SEI形貌进行了表征,以进一步探讨LiNO3对锂阳极的影响。在电解液中加入LiNO3后,锂阳极表面SEI的形貌和结构发生了明显的变化。在1M LiTFSI-DOL/DME电解质中循环的锂显示出粗糙和多孔的形态(图1c)。锂在含有2% LiNO3的电解质中循环,其表面形貌平滑,呈结节状堆叠(图1d)。形态差异表明,LiNO3的加入有助于在锂表面形成致密和光滑的SEI,并且致密的SEI可以有效地防止电解质与锂反应,从而导致Li| |Li电池的更长的循环寿命。
三、锂浸入电解质时锂/电解质界面的反应
SEI起源于锂和电解质组分之间的反应。因此,通过原位衰减全反射傅里叶变换红外光谱(ATR-FTIR)测量,进一步研究了锂表面SEI的组成以及锂与电解质之间的界面反应。
红外光谱直接证明了LiNO3加速了LiTFSI和溶剂的还原,从而锂浸泡在含LiNO3的电解质中形成了致密而稳定的SEI。在1 M LiTFSI-DOL/DME的浸泡过程中观察到一些向下的峰(图2a),包括对应于LiTFSI的O=S=O键断裂的1355和1335cm-1处的峰,以及1059和1184/1125cm-1处的峰分别表明LiTFSI的S–N–S和C–F键的裂解。此外,在700 cm-1处出现明显的向上峰,表明在锂电极的SEI上形成类–C(S=O)C–结构,这可能来源于LiTFSI的分解(图2a)。在原位红外光谱中还观察到锂表面溶剂的分解。在1082 cm-1的下行峰归因于溶剂的C–O键表明DOL的开环反应,并且在1456 cm-1处的向下峰揭示了溶剂的C–H键的裂解(图2a)。此外,DOL的分解产物为类ROLi物种,如由C–O和C–O–C引起的1010和836 cm-1的上升峰所示(图2a)。上述下降峰的强度在前30 min迅速降低,然后缓慢下降,表明浸没在没有LiNO3的电解质中的锂电极表面上的LiTFSI和DOL分解缓慢(图2b)。在1058和1186 cm-1处的明显向下峰显示,在2% LiNO3的电解液中更多的LiTFSI的S–N–S和C–F键在锂表面断裂(图2a)。LiNO3电解质中向下峰的强度演变也与1 M LiTFSI-DOL/DME电解质中的强度演变有很大不同(图2c)。下降峰的强度在最初的15 min迅速下降,然后在接下来的15 min减慢,随后从30 min到60 min又迅速下降,表明电解质进一步分解。在原位红外光谱中没有观察到LiNO3的特征峰,可能是由于其低浓度和高反应活性。
上述光谱分析表明,DOL、LiTFSI和LiNO3会在OCV的锂表面分解,这与其他报道不同,可能是由于在本研究中OCV静息处理时间较长所致。另外,LiNO3还可以促进电解质特别是LiTFSI还原成小分子,从而在锂表面形成更稳定的SEI。
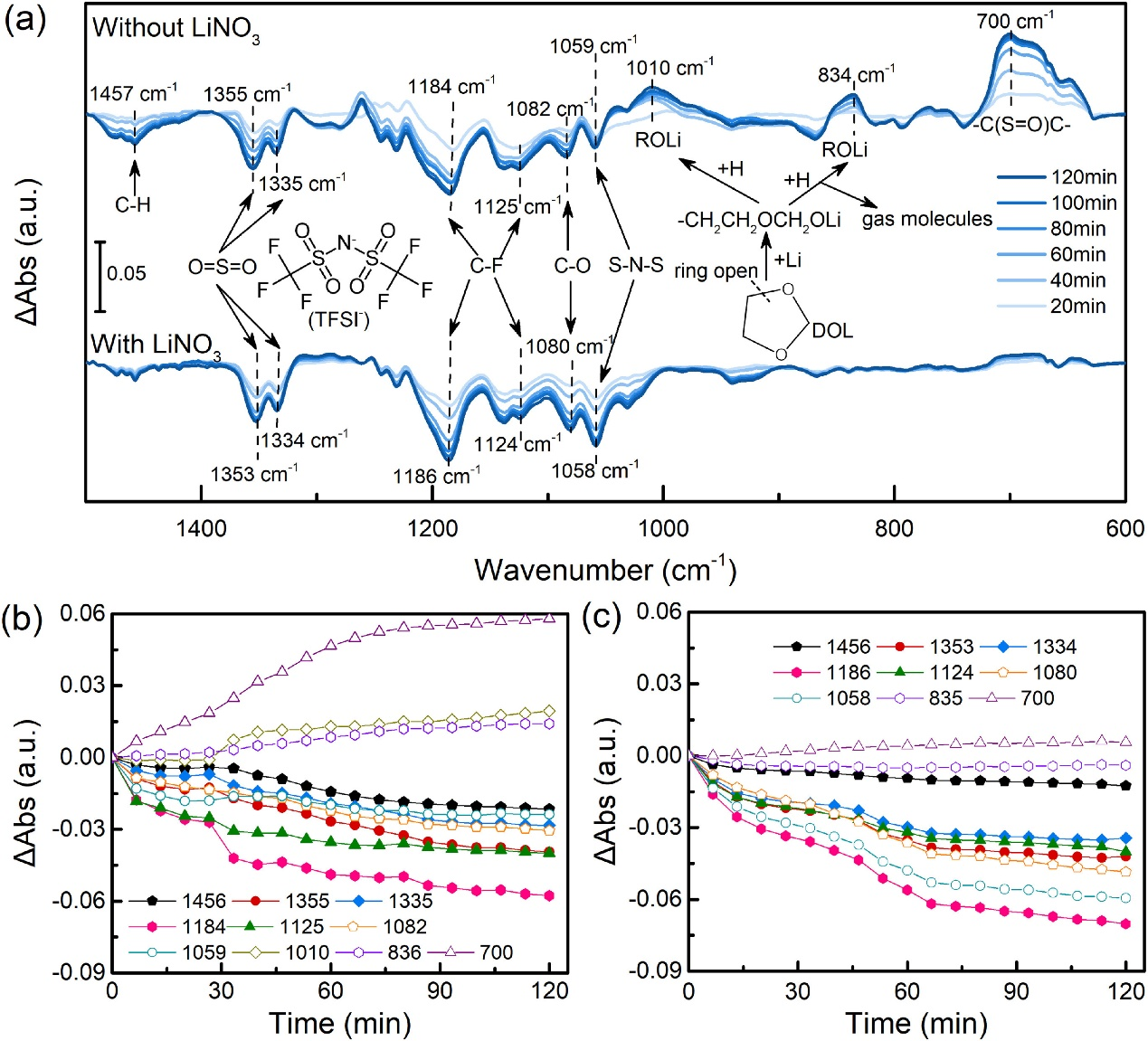
图 2. (a) 锂电极在不同电解质中的原位ATR-FTIR光谱演变。(b) DOL/DME中1 M LiTFSI和(c) 具有2 wt% LiNO3的DOL/DME中1 M LiTFSI的选定FTIR峰强度的变化。
四、电解液在锂表面的还原过程
在原位光谱化学分析的基础上,采用密度泛函理论(DFT)的AIMD模拟方法进一步研究了SEI在锂电极表面的界面反应和形成机理。从不同AIMD模拟时间获得的构型直接观察到LiTFSI的还原途径。在1 M LiTFSI-DOL/DME的无 LiNO3电解质中(图3),LiTFSI首先在0.460 ps处还原,N–S键断裂形成–NSO2CF3和–SO2CF3基团。在随后的模拟过程中,–NSO2CF3基团在锂表面保持稳定,而形成的–SO2CF3基团在–CF3基团的C–F键先后在0.590、0.905和1.000 ps处断裂后,随着C–S键在0.475 ps处断裂而进一步减少。同时,S=O2基团的S=O键也在0.950和1.510 ps处裂解。在1 M LiTFSI-DOL/DME电解质中锂表面上TFSI-的还原途径与LiTFSI/DOL混合物中的另一报道一致。
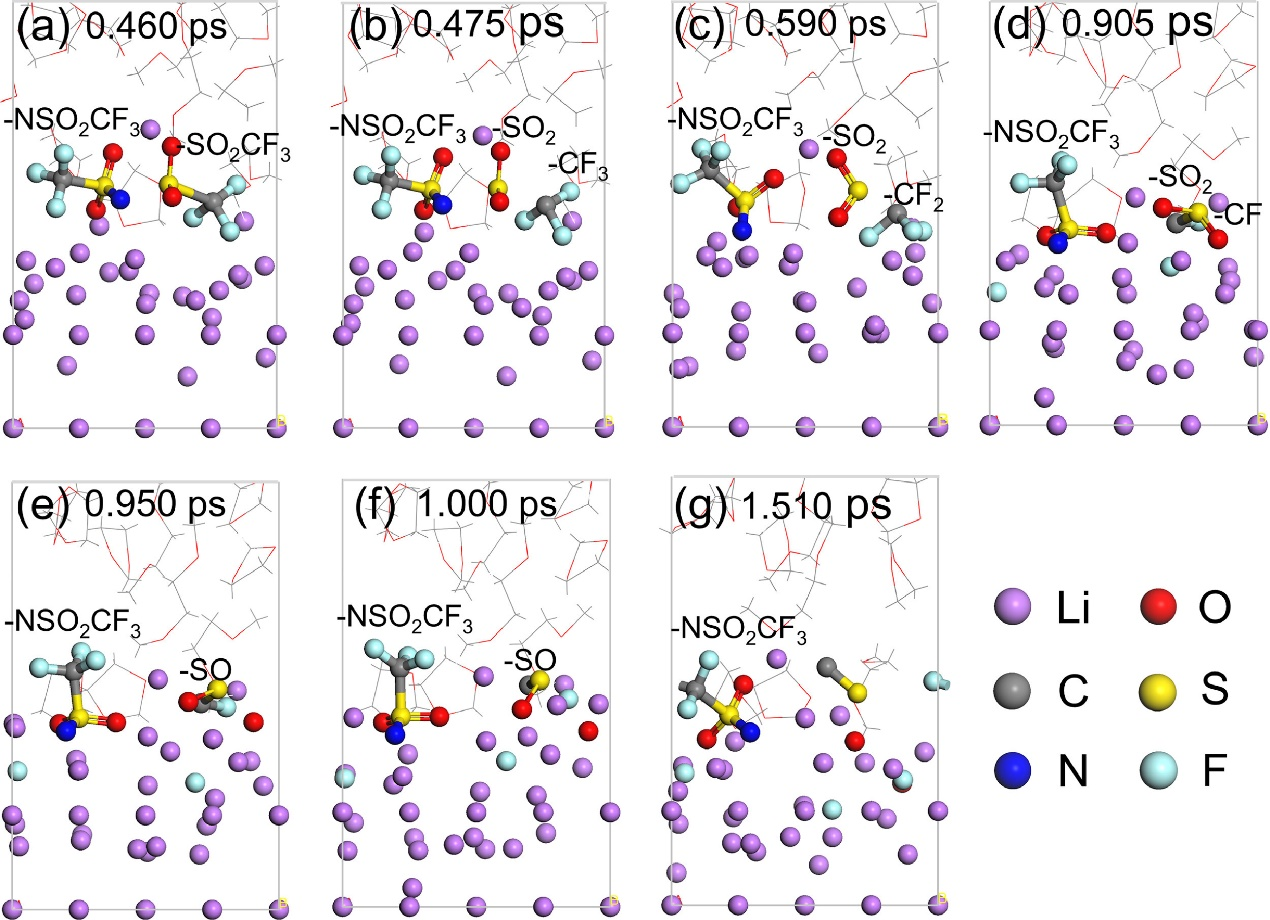
图 3. 在不同AIMD模拟时间下,不含LiNO3的DOL/DME中1 M LiTFSI还原过程。溶剂分子被简化为棒状模型。
另外,通过N–S和C–S键的断裂,LiTFSI在0.439 ps 时直接还原为–NSO2CF3,–SO2和–CF3基团(图4),–CF3基团的C–F键随后以0.457、0.811和0.982 ps断裂,并且–SO2基团也随着以1.017和1.353 ps断裂两个S=O键而减少。在AIMD模拟过程中,在含有2% LiNO3的电解质中形成的–NSO2CF3基团不断减少(图4)。在5.420 ps时,C–S键断裂,–NSO2CF3基团还原,形成–CF3和–NSO2基团,–CF3基团的C–F键断裂时间分别为6.280、6.972和7.000 ps,而–NSO2基团在锂表面保持完整,DOL和DME的一些溶剂分子也被还原,并且在两种电解质体系中观察到DOL分子的开环反应,这表明在锂阳极附近形成了短链–O(CH2)2O (CH2)3OCH2O–物种。
LiNO3的加入导致LiTFSI在锂表面能够完全还原,从而形成一个紧凑而稳定的SEI。在这两种电解质体系中,表面附近的松弛锂原子从原来的位置移出,表明它们参与了盐和溶剂的还原。在含LiNO3的电解质中,LiTFSI和LiNO3几乎完全分解在锂表面形成–NSO2的最大碎片(图4j)。因此,在有LiNO3存在的情况下表面更为致密。另外,在LiNO3存在下,由于10ps后LiTFSI中NO3-的完全分解和C–F键的断裂,形成了更多的Li2O和LiF。AIMD模拟过程的直接产品也可以构成SEI的组成部分。
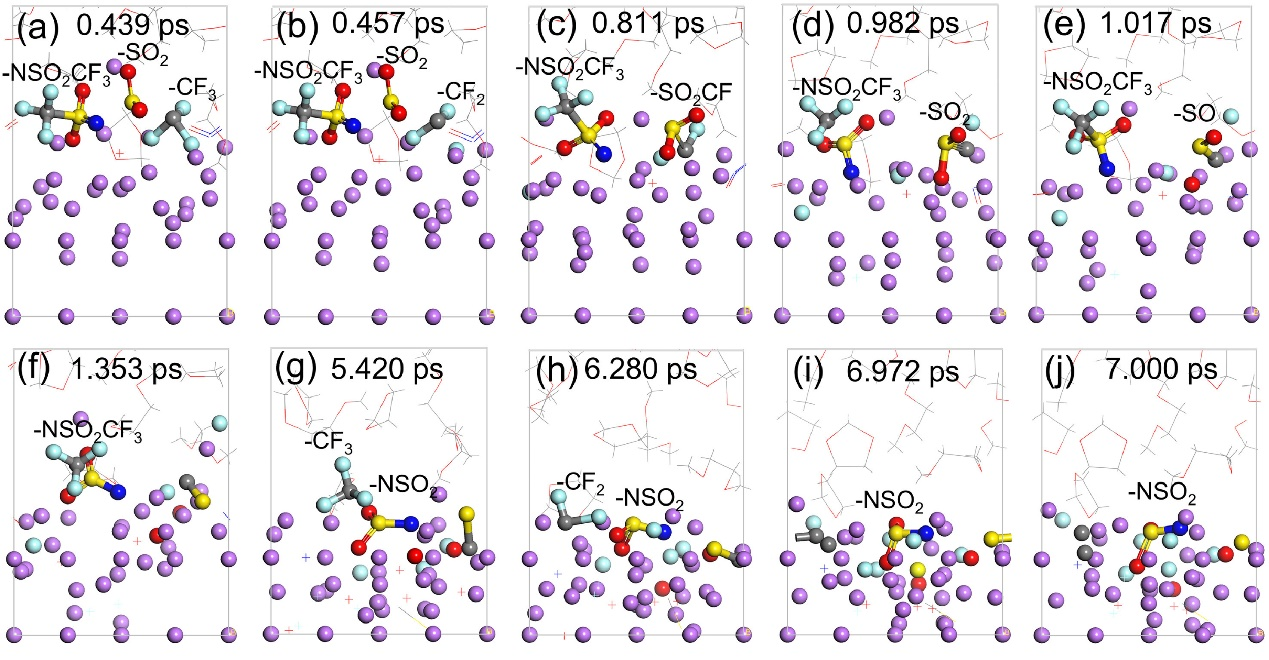
图 4. 在不同AIMD模拟时间下,含有2 wt% LiNO3的DOL/DME中1 M LiTFSI还原过程。溶剂分子被简化为棒状模型。
五、锂沉积和溶出过程中锂/电解质界面的动态过程
根据锂电极在不含LiNO3的电解液中沉积和溶出过程中的原位红外光谱(图5a) ,可以观察到TFSI-的连续分解和电迁移。在阴极扫描过程中,观察到LiTFSI在1356、1336、1186和1059 cm-1处有四个向下的峰值,分别对应于LiTFSI的O=S=O,C–F和N–S键,并且当阴极电位从0.9 V扫描到0 V时,强度显著降低,表明锂阳极附近的LiTFSI发生了分解(图5c)。在0 ~ 0.3 V范围内,随着阴极极化的进一步加深,这些峰的强度增加,这可能是由于TFSI-在锂阳极表面的吸附所致。
在含2% LiNO3电解质的1 M LiTFSI-DOL/DME中,锂沉积/溶出过程的FTIR光谱与无LiNO3电解质中的FTIR光谱有很大不同。在大约1086 cm-1的峰值显著下降,然后在整个阴极和阳极扫描稳定下降,表明溶剂的连续分解(图5b和d)。在阴极从0.9扫描到0 V期间,TFSI-的峰值在1353、1333、1189和1061 cm-1(图5b)强度保持稳定,由于TFSI-的吸附而增加到0.3 V的最高值(图5d)。在接下来的阳极扫描过程中,峰值强度从0.3 V迅速下降到0 V,然后缓慢下降(图5d)。结果表明,在锂的沉积/溶出过程中,TFSI-的分解速率非常缓慢,峰出现在1210 cm-1处,这可以归因于TFSI-和DOL之间的反应而在SEI中形成类ROSO2Li组分(图5b)。在随后的阴极扫描和阳极扫描过程中,这一向上的峰值不断增加,而在阳极扫描过程中逐渐减小,表明SEI中的类ROSO2Li组分是在锂沉积过程中形成的,随后在锂溶出过程中分解成小分子或扩散开来。
通过对锂沉积/溶出过程中原位红外光谱的分析表明,锂离子与溶剂的反应产物类ROSO2Li组分构成了SEI的新组分。此外,在含有LiNO3添加剂的电解质中,在放电过程中形成新的SEI组分,并在充电过程中再次分解或扩散,维持SEI的动态形成/溶解平衡。结合原位红外光谱分析结果,可以得出结论: LiNO3可以促进SEI的形成,使SEI更加稳定和致密。在浸泡过程中形成的稳定的SEI阻碍了电解质在含LiNO3电解质中的锂沉积/溶出过程中的还原和分解,从而导致电池的高库仑效率和长期循环稳定性。
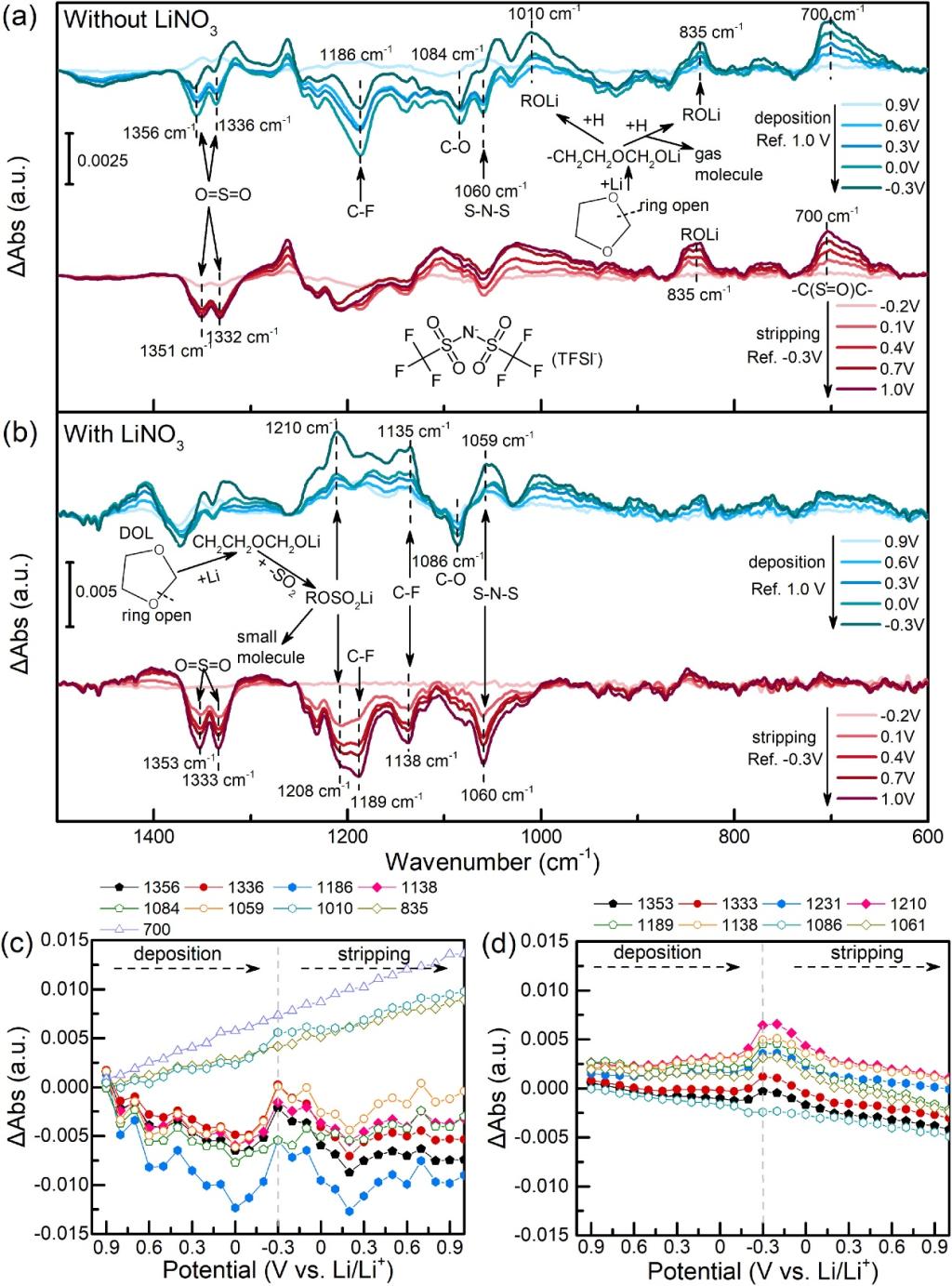
图 5. (a) 锂电极在不同电解质中沉积和剥离过程中在不同电位下的原位ATR-FTIR光谱。(b) DOL/DME中1 M LiTFSI 和(c) DOL/DME中2 wt% LiNO3中1 M LiTFSI 在锂沉积和剥离过程中所选择的FTIR峰的不同电位处的强度演变。
六、循环锂电极SEI的化学分析
为了进一步阐明LiNO3在长期循环过程中SEI组分变化中的作用,我们进行了XPS表征来研究循环锂电极的化学组分。在循环锂中观察到大约531.3 eV的O 1s峰归因于Li2O的电极(图6a),在LiNO3电解质中循环的锂电极的Li2O比率略高于不含LiNO3的电解质(14.8%比13.3%)。然而,两个循环锂电极之间的O含量差异并不明显,这可能与电解液中LiNO3含量较低有关。实际上,当LiNO3的浓度增加时,循环锂中O的含量差异会更大。此外,SEI的无机组分主要形成在内层,而循环锂电极的XPS光谱反映了更多关于SEI接近电解质性能的信息。在LiNO3电解液中循环锂的F、N和S含量略低于没有LiNO3的电解液中的含量,这种差异可能是由于在锂沉积和溶解的100个循环中,LiTFSI在LiNO3电解质中的分解较少造成的,F 1s、N 1s和S 2p光谱的相对强度进一步证明了这一点(图6)。
XPS分析结果表明,在长期的锂沉积/溶出过程中,电解液中添加LiNO3可以降低锂的TFSI-。由于电解质的还原与SEI的组成和稳定性直接相关,这表明LiNO3添加剂可以促进稳定SEI的形成,抑制LiTFSI与锂电极之间不良的进一步反应。此外,锂电极上的SEI由无机成分(包括Li2O、 LiF、 Li2SOx、Li2S)和有机分子(如RSOx)组成。此外,Li2O对改善锂电极的电化学性能有重要作用。
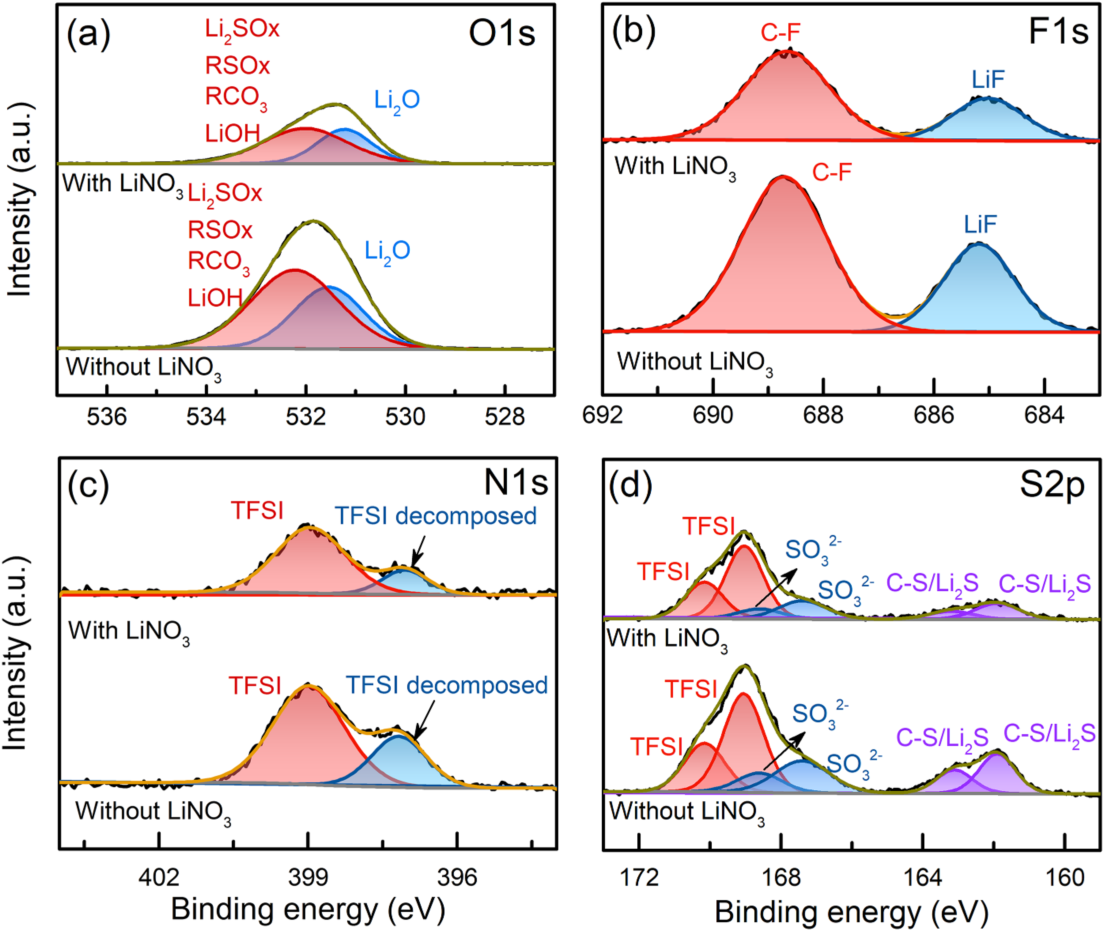
图 6. 在不同电解质中循环的锂各种元素的高分辨XPS光谱: (a) O 1s, (b) F 1s, (c) N 1s, (d) S 2p。
在上述原位FTIR光谱和AIMD模拟研究的基础上,提出了LiNO3添加剂对SEI演化的总体影响(图7)。当锂电极浸入电解质中时,一些DOL分子被具有开环反应的锂还原,在锂表面形成ROLi和HCO2Li样的SEI组分。随着LiNO3在电解质中的加入,由于其高反应性,LiNO3被还原成Li2O或LiNOx物种,并且LiTFSI被彻底还原成LiF,Li2O和其他在原位FTIR光谱中不敏感显示的小分子或可溶性分子。在循环锂沉积/溶出过程中,LiTFSI和溶剂在无LiNO3电解质中不断分解(图5a),在 LiNO3添加剂的电解液中,LiTFSI的分解速率受到阻碍,并且在锂沉积过程中LiTFSI与DOL溶剂发生反应,导致ROSO2Li的一些新的SEI组分出现,然后在锂溶出过程中再次分解或扩散(图5b)。结果表明,LiNO3添加剂可以促进LiTFSI的彻底分解,从而形成稳定和致密的SEI。而在不含LiNO3的电解质中形成的SEI是多孔和不稳定的(图1c和d)。在含LiNO3电解质中稳定的SEI抑制了电解质的锂沉积/溶出过程中的副反应,从而提高了电池的库仑效率和长期循环稳定性。
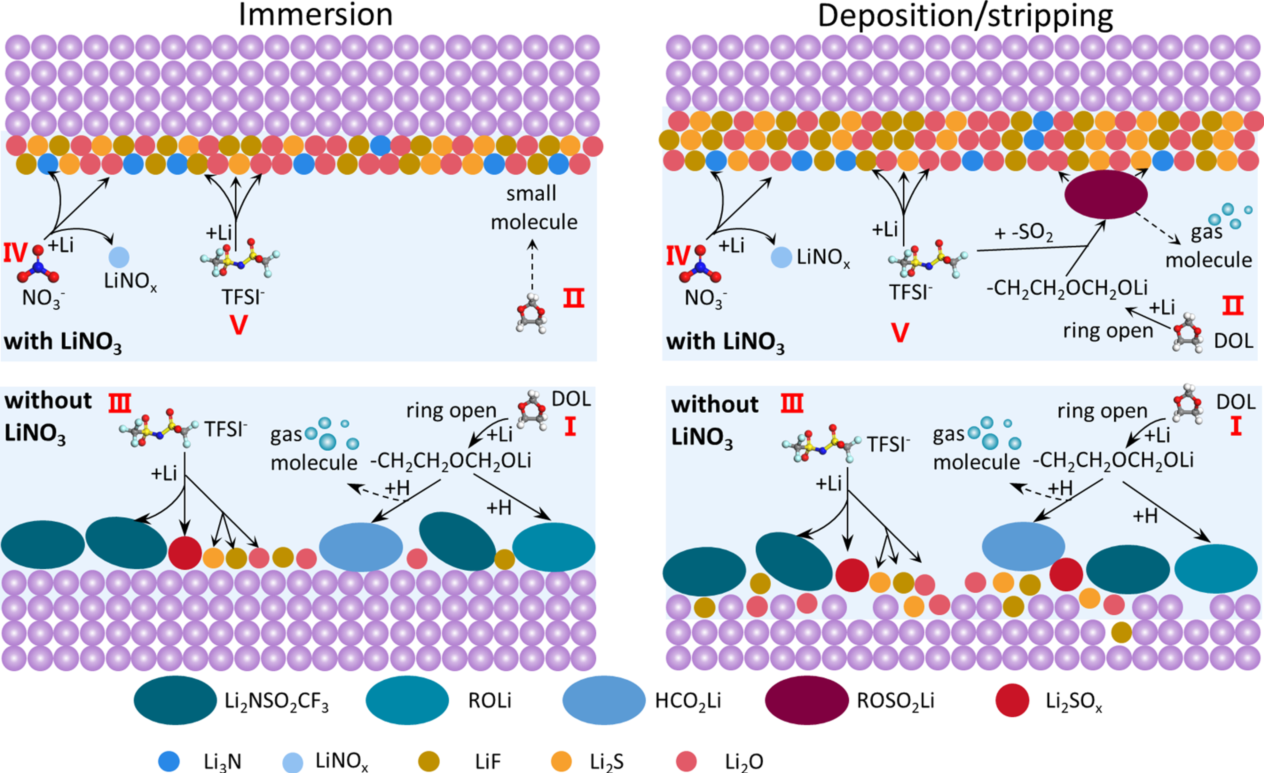
图 7. 提出含和不含LiNO3电解液中锂负极表面SEI逸出的机制。
结论
我们通过原位ATR-FTIR光谱表征和AIMD模拟揭示了添加剂在界面反应和锂电极表面SEI动态形成中的作用。在锂电极上加入LiNO3可以观察到不同的SEI动力学行为。在含LiNO3的电解质中,LiNO3促进了LiTFSI的彻底还原,形成了一种由Li2O、LiF、Li2SOx、Li2S等无机组分以及一些有机分子组成的致密而稳定的SEI。此外,在含有LiNO3的电解质中,在锂沉积/溶出过程中直接观察到SEI的动态形成/溶解平衡。稳定的SEI阻碍了在含LiNO3电解质中锂沉积/溶出过程中的副反应,从而提高了电池的库仑效率和长期循环稳定性。此外,在含LiNO3的电解液中,SEI中发现了更多的Li2O组分,这可能对醚基电解液中锂阳极的稳定起主导作用。然而,在不含LiNO3的电解质中,当锂浸泡在电解质中时,会形成不稳定的SEI,并且电解质分子在整个锂沉积/溶出过程中不断分解。这项研究为进一步认识LiNO3在锂电极SEI动态形成中的作用提供了新的视角。
作者简介

武龙胜,博士,华中科技大学环境学院毕业,博士研究方向为锂硫电池性能研究

胡敬平,博士、教授,华中科技大学环境学院。博士毕业于英国牛津大学化学系,博士毕业后先后在英国诺丁汉大学和牛津大学从事博士后研究,荣获Ramsay Fellowship。目前主要研究方向为环境催化、环境功能材料和固废资源化与污染控制技术。在Adv. Mat.、Adv. Func. Mat.、Angew. Chem.等期刊发表论文190余篇,单篇最高他引210余次,总他引超过6000次,H因子44。担任“Energy & Environmental Materials”期刊副主编、巴塞尔公约亚太区域中心化学品和废物环境管理智库专家、湖北省资源综合利用协会专家委员会委员,主持国家重点研发课题、国基金、省基金重点项目,承担科技部青年973项目。
文献链接
Longsheng Wu, Jingping Hu*, Sijing Chen, Xiaorong Yang, Lu Liu, John S. Foord, Paulius Pobedinskas, Ken Haenen, Huijie Hou, Jiakuan Yang, Lithium nitrate mediated dynamic formation of solid electrolyte interphase revealed by in situ Fourier transform infrared spectroscopy, Electrochimica Acta, 2023,466,142973.
(https://doi.org/10.1016/j.electacta.2023.142973)

课题组主页:http://funmat.ese.hust.edu.cn/

